2025年10月10日,广州医科大学李斌团队、中国医学科学院北京协和医学院肿瘤医院刘芝华团队、广州医科大学许雯雯团队、上海交通大学医学院附属胸科医院李志刚团队、中国医科大学王振宁团队合作在Nature Genetics发表题为Single-cell multi-omic and spatial profiling of esophageal squamous cell carcinoma reveals the immunosuppressive role of GPR116⁺ pericytes in cancer metastasis 的研究论文。
该研究整合单细胞多组学及时空组学技术Stereo-seq,系统绘制了食管鳞癌促转移TME的单细胞空间图谱,鉴定出一个由转录因子PRRX1驱动、具有显著免疫抑制功能的GPR116⁺周细胞亚群,并阐明其通过EGFL6-integrin β1-NFκB轴促进肿瘤转移的分子机制。该研究进一步发现血清EGFL6可作为多种癌症的诊断和预后生物标志物,而靶向integrin β1则可有效抑制转移并增强免疫治疗效果,为未来临床干预提供了新策略。

在该研究中,时空转录组检测采用了华大时空组学技术Stereo-seq,华大智造DNBSEQ测序平台为该研究的基因测序提供了支持。蛋白多重免疫荧光mIF检测采用了2000RS FluoXpert 系统,通过自动化流程完成多重免疫荧光染色与成像。该系统可通过 “染色 - 成像 - 洗脱” 循环实现快速高效的多重免疫荧光染色,每个循环检测2种标志物。通过抗体洗脱使组织恢复初始状态,以便进行后续循环。
为了对肿瘤微环境进行深度解析,作者设计了一个8-plex Panel,即在同一张切片上进行8个标记物的多重荧光染色,并将所得图像在FluoXpert Vision分析平台上进行多通道观察及分析。分析结果显示,PD-1⁺ CD8⁺ T细胞与Tregs在GPR116⁺ 周细胞周围显著富集,呈现出高度空间相关性;这一免疫抑制性微环境在发生转移的ESCC患者中更加突出。该结果结合单细胞多组学与多重荧光定量分析技术,为揭示肿瘤免疫逃逸与转移微环境提供了强有力的证据。
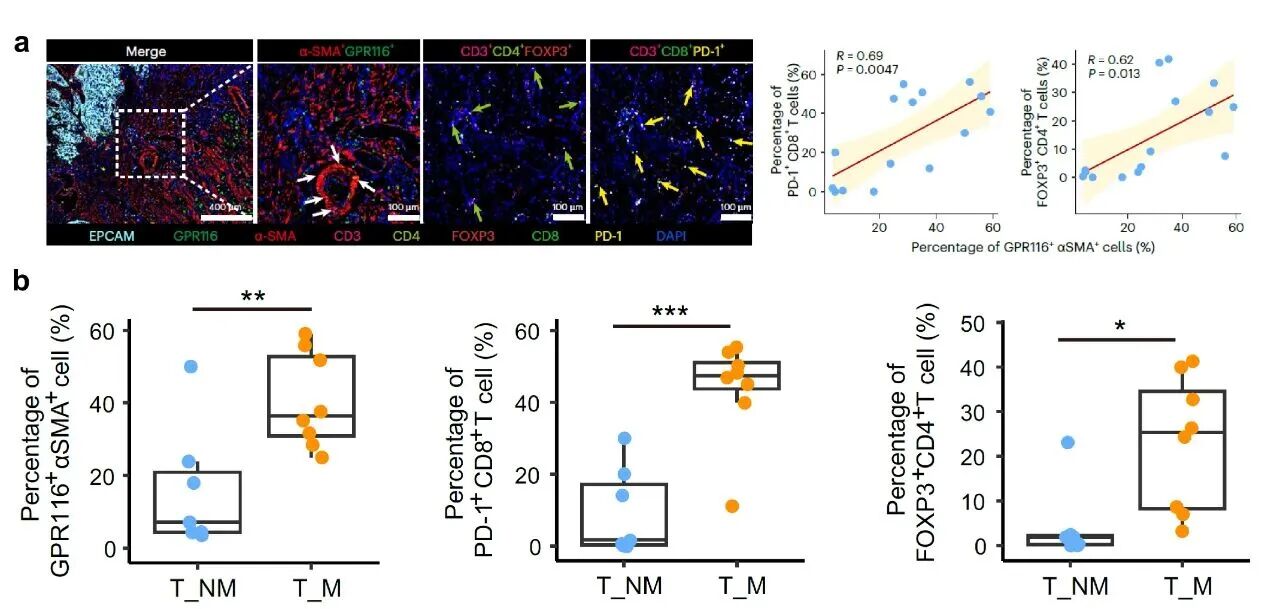
图示:(a)食管鳞状细胞癌(ESCC)肿瘤组织中细胞亚群的多重免疫荧光染色示例(左图)及相关性分析(右图)(b)根据多重免疫荧光染色结果统计出发生转移(T_M)和无转移(T_NM)的 ESCC 患者肿瘤组织中不同细胞类型比例对比 (8-Plex Panel: EPCAM, GPR116, α-SMA, CD3, CD4, FOXP3, CD8, PD-1.)
肿瘤转移是导致癌症患者死亡的主要原因。然而,肿瘤微环境(TME)中的细胞多样性及其相互作用如何促进转移仍不完全清楚。食管癌发病隐匿,超过50%的患者在初诊时已发生转移,患者5年总体生存率仅约20%,亟需深入解析原发位点TME促进肿瘤细胞转移的关键机制并发现新的治疗靶点和生物标志物。周细胞是嵌于血管基底膜中的壁细胞,在血管发育和重塑中发挥重要作用。近期研究表明,在结直肠癌、肺腺癌等肿瘤中,周细胞比例相较于正常组织有所增加,暗示其与肿瘤进展相关,但周细胞在肿瘤免疫和转移进程中的功能异质性仍有待深入探索。
通过单细胞多组学和空间转录组分析,研究者发现在转移患者的肿瘤微环境中,周细胞与上皮细胞的相互作用显著增加,且空间距离更加靠近,提示周细胞在ESCC转移中可能发挥关键作用。通过对周细胞进行进一步亚群分析,研究者首次鉴定出GPR116⁺周细胞,并发现其在转移患者中显著富集,其比例与患者较差生存率显著相关。研究者进一步筛选出GPR116⁺周细胞转化的上游关键转录因子PRRX1,并通过周细胞特异性Prrx1敲除小鼠证实PRRX1是GPR116⁺周细胞分化的必要条件。
空间分析表明在转移患者中,GPR116⁺周细胞更靠近肿瘤边缘,并与高EMT潜能的肿瘤细胞密切接触。细胞实验和多个小鼠转移模型均证明GPR116⁺周细胞可显著促进ESCC转移。EGFL6是GPR116⁺周细胞中最特异高表达的基因,可显著促进肿瘤细胞的侵袭和EMT进程。EGFL6水平与患者较差预后相关。血清EGFL6水平可有效区分健康人与ESCC患者、以及非转移与转移患者, 在肺癌和胃癌中也得到验证,表明其在肿瘤早筛预测和预后中作为非侵入性生物标志物的潜在效能。机制方面,GPR116+周细胞通过EGFL6与肿瘤细胞上的integrin β1结合并激活下游NFκB通路, integrin β1抑制剂或NFκB抑制剂均可阻断EGFL6的促侵袭效应。在多个ESCC小鼠模型中,使用integrin β1抗体均可显著抑制肿瘤转移。

综上所述,本研究鉴定出一个全新的GPR116⁺周细胞亚群,在肿瘤微环境中作为关键驱动细胞促进食管鳞癌转移,同时通过进一步挖掘其上游分化机制和下游促转移分子机制,开创性地提出跨癌种的非侵入性肿瘤诊断和转移预后的血清生物标志物,及靶向integrin β1同时遏制转移和免疫抑制的新型干预策略,为改善食管癌及其他实体瘤患者的临床预后提供了重要的理论依据与转化路径。



