重度耳聋患者通常依赖人工耳蜗,但对于内耳或听神经严重损伤的患者,人工耳蜗往往效果不佳。虽然听觉脑干植入等脑机接口技术已实现临床应用,但因耳蜗核结构复杂、编码机制不清,患者术后言语理解能力仍普遍有限。如何精准定位耳蜗核中的功能靶点,已成为突破听觉脑机接口疗效瓶颈的关键挑战。
2026年4月6日,Cell Research在线发表了由上海交通大学医学院附属第九人民医院联合深圳华大生命科学研究院完成的重要研究成果。研究人员基于华大智造的时空组学技术(Stereo-seq)、单细胞核RNA测序(snRNA-seq)与单细胞核ATAC测序(snATAC-seq),成功绘制了全球首个小鼠耳蜗核高分辨率单细胞空间转录组图谱。
其中,snRNA-seq与snATAC-seq文库均基于华大智造DNBelab C系列平台构建,所有测序均在DNBSEQ-T7或DNBSEQ-T1平台上完成。该研究不仅精细解析了听觉“中继站”的细胞与空间构成,更首次揭示基因Spp1是听觉活动依赖的核心分子,对维持正常的听觉信息处理速度不可或缺。这一发现为理解听觉发育和感音神经性耳聋的病理机制提供了全新的分子与细胞框架。

在以往的听觉研究中,耳蜗核内部复杂的细胞类型及其精确的空间排布关系,如同一个未被解密的“黑箱”。而本研究通过将时空组学技术与单细胞多组学测序技术深度融合,实现了对小鼠耳蜗核的跨尺度解析。
通过Stereo-seq技术,研究人员可以像使用“分子显微镜”一样,在空间原位观测耳蜗核的基因表达模式,并通过对空间数据的细胞分割,精准解析了超过21万个单细胞的转录组信息及其空间位置。同时,单细胞核RNA测序(snRNA-seq)技术则提供了更深度的单个细胞转录组数据,用于细化细胞类型鉴定。
通过这种整合,研究团队成功构建了小鼠耳蜗核的单细胞空间转录组整合图谱。研究中主要使用了 BIN50(约25 µm × 25 µm) 的分辨率来定义耳蜗核亚区。这个尺度足以覆盖多个相邻细胞,从而清晰地识别出具有不同基因表达谱的亚区域。基于此,研究首次从分子层面系统定义了13个分子亚区,并聚类出20种主要细胞类型,精细描绘了听觉信息初步处理的细胞与分子蓝图。
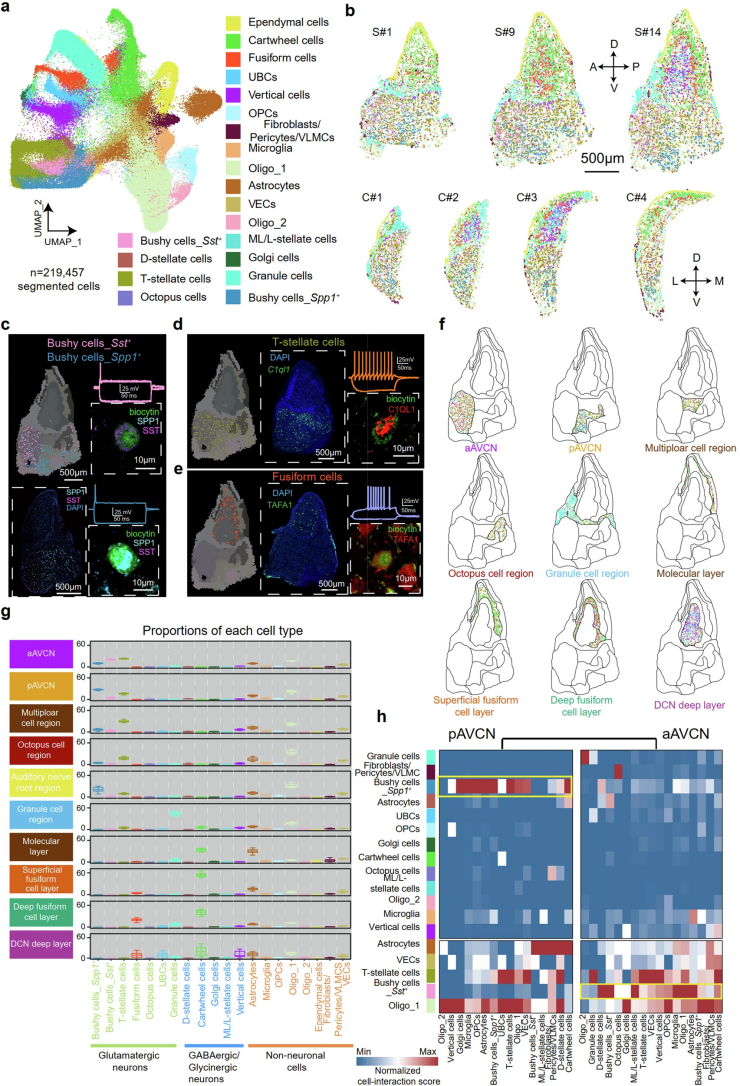
图1. 基于Stereo-seq技术鉴定的小鼠耳蜗核细胞类型及其空间细胞图谱
研究团队深入探究了听觉经验如何塑造耳蜗核。通过分析多种先天性耳聋小鼠模型的转录组数据,团队发现听觉输入能显著调控耳蜗核细胞的基因表达程序,且丛状细胞对听觉剥夺最为敏感。该程序在正常听力小鼠中高度活跃,在耳聋模型中显著下调,并在听力恢复后部分回升,证明其表达直接受听觉输入调控。
同时,利用细胞特异性基因网络对这些细胞在听力损失时进行了更深入的分子特征分析,发现Spp1是核心基因。由于Spp1是空间转录组数据中丛状细胞的主要标记基因,因此Spp1+丛状细胞是听觉输入变化最敏感的细胞亚型。
空间组学分析进一步揭示,听觉不仅调控基因表达,还重塑细胞微环境:在耳聋小鼠中,Spp1+丛状细胞与邻近小胶质细胞间的距离异常缩短。单细胞数据细胞间通讯分析也表明和WT(野生型小鼠)样本相比,VGLUT-/-小鼠样本中Spp1+ 丛状细胞与小胶质细胞之间通讯强度降低,VGLUT-/-+GT样本(基因治疗小鼠)中Spp1+丛状细胞与小胶质细胞之间通讯强度增强。这表明听觉输入可能通过调控非神经元细胞的空间位置来间接影响神经元功能网络。
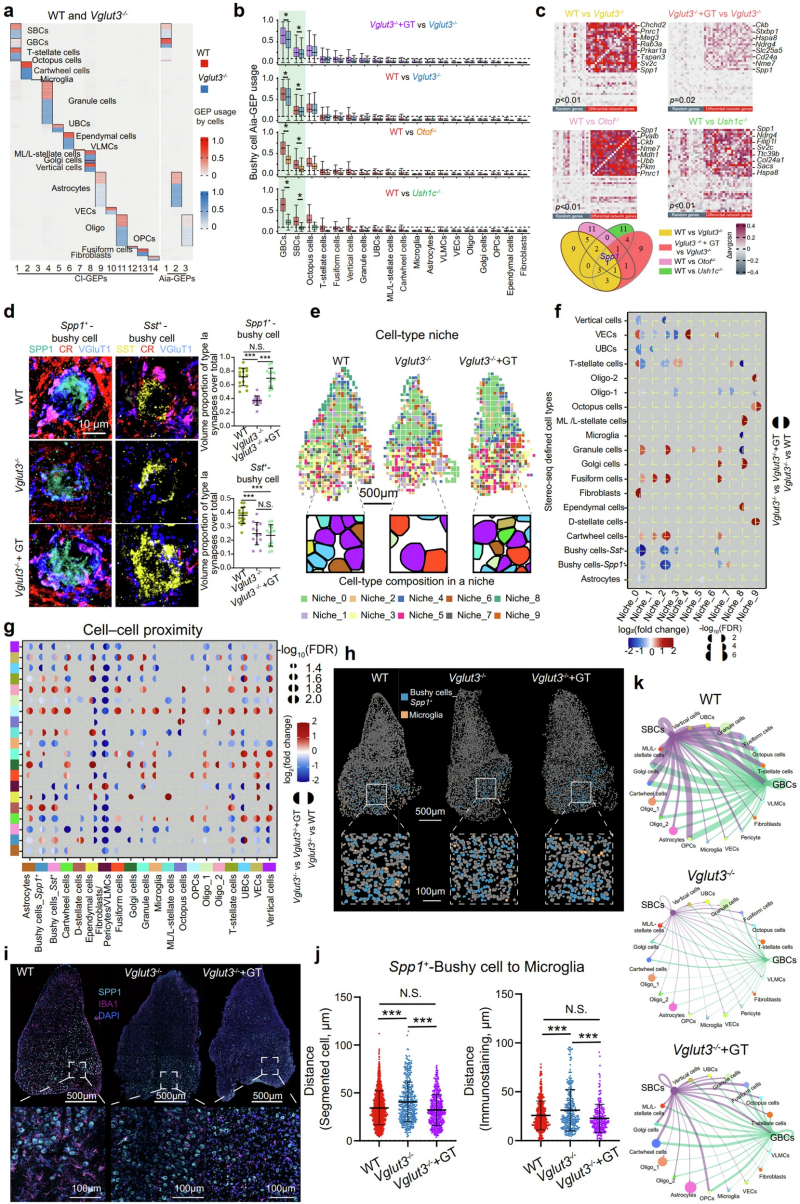
图2. Spp1+丛状细胞被确定为对听觉刺激表现出转录组和空间关系响应的主要细胞类型
3. 功能验证:Spp1是维持听觉信息处理速度的关键
为验证Spp1的作用,研究者构建了基因敲除小鼠。敲除后小鼠听阈正常,但听性脑干反应中Ⅱ、Ⅲ、Ⅳ波的潜伏期延长,表明耳蜗核及上游听觉通路信息处理变慢。电生理记录显示,敲除小鼠的丛状细胞自发性兴奋性突触后电流幅度降低,上升和衰减时间延长,突触传递效率下降。同时,与神经元发育和突触相关的多个基因表达下调,神经元胞体面积减小,说明Spp1是维持耳蜗核正常听觉功能的关键分子。
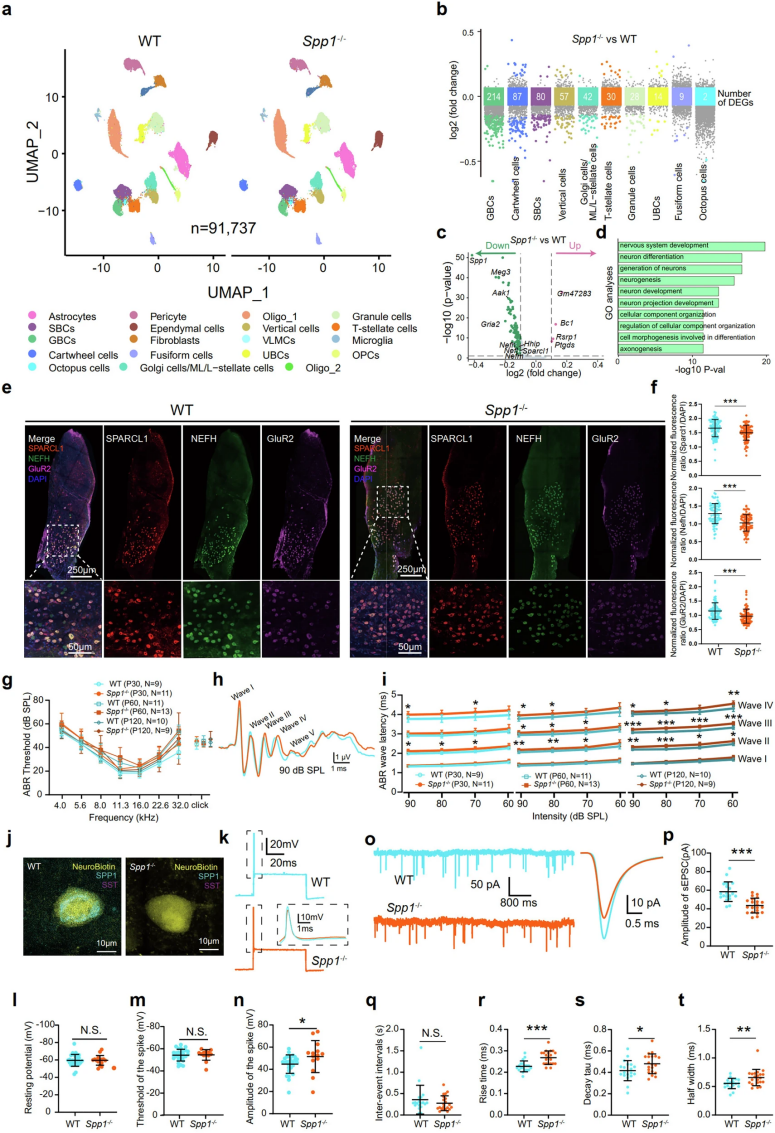
图3. Spp1是维持Spp1⁺丛状细胞正常功能所必需的
本研究是时空组学技术驱动脑科学向微观纵深发展的一个生动例证。借助Stereo-seq高分辨率技术,研究人员首次得以在单细胞层面清晰“看见”并系统解析耳蜗核的精细细胞结构及其听觉依赖的动态变化。这一突破不仅深化了对听觉中枢基本机制的理解,更重要的是,它通过锁定Spp1⁺丛状细胞及其关键基因Spp1这一靶点,直接将基础研究发现与优化听觉脑干植入等临床治疗策略联系起来,为从分子层面干预中枢听觉可塑性、提升听力康复效果提供了全新的科学思路。
该研究由上海交通大学医学院附属第九人民医院、上海交通大学医学院耳科学研究所、上海市耳鼻疾病转化医学重点实验室牵头联合华大生命科学研究院共同完成,上海交通大学医学院附属第九人民医院吴皓教授为本论文唯一通讯作者,上海交通大学医学院附属第九人民医院刘辉辉博士、深圳华大生命科学研究院廖上峰生物信息副研究员、李小苇生物信息副研究员、宋历博士为本文的共同第一作者。




