胰腺导管腺癌(PDAC)素有 “癌中之王” 之称,传统化疗与免疫治疗疗效有限,其核心原因在于肿瘤被高度致密且异质的纤维化基质所包裹。肿瘤相关成纤维细胞(CAFs)曾被普遍认为是促瘤 “帮凶”,但动物实验显示,单纯清除CAFs反而会加速肿瘤进展,提示CAF群体内部存在功能截然不同的细胞亚型。
目前,肌成纤维型、炎症型等促瘤性CAF亚群已被陆续鉴定,而发掘并阐明具有抑瘤功能的CAF亚型及其调控机制,已成为该领域亟待解决的关键科学问题。
近日,北京大学第一医院和美国约翰斯·霍普金斯大学医学院等研究团队合作,在国际消化病学期刊Gut上发表研究成果。研究成功鉴定出一种全新的、具有抑瘤功能的CAF亚群。因其高表达补体通路相关基因,被命名为“分泌补体的CAF”(csCAF)。
研究通过整合单细胞多组学和时空组学技术Stereo-seq等发现,csCAF与另一种已知的促瘤性CAF(iCAF)关系密切,可能是其“未激活”的早期状态。更重要的是,临床数据分析显示,肿瘤组织中csCAF比例较高的胰腺癌患者,其总生存期和无复发生存期显著更长,提示csCAF与良好预后相关。

点击图片阅读原文
样本类型:人类PDAC原发灶,还纳入正常胰腺、癌前病变、其他胰腺肿瘤及肝/肺转移灶样本,同时结合小鼠模型和公开数据进行了跨物种验证;
核心技术:单细胞转录组测序(scRNA-seq)、单细胞核多组学测序(snMultiome-seq)、空间转录组测序(Stereo-seq)、多重免疫组织化学(mIHC)、批量RNA测序(bulk RNA-seq)等;
样本规模:研究通过单细胞RNA测序(scRNA-seq)分析了15 例自建人源样本,并整合了263 例公共数据集样本进行联合分析;利用单核多组学测序(snMultiome-seq)分析10例样本;通过时空组学技术(Stereo-seq)分析5例样本;并采用空间原位分析技术对5例瘤变样本进行检测。此外,本研究还回顾性收集了化疗初治及经治两个临床队列,用于后续临床相关性分析。
关键研究内容
发现“守护者”:补体分泌型CAF
研究团队利用单细胞多组学技术,对胰腺癌样本进行了高精度解析,成功在成纤维细胞群体中,发现了一个前所未有的新亚群。这个亚群高表达补体通路相关基因,因此被命名为补体分泌型CAF(csCAF)。
研究进一步揭示了csCAF与促瘤亚型炎症性CAF(iCAF)之间微妙而关键的关系。两者在转录谱和表观遗传特征上存在大量重叠。通过伪时序分析和RNA速率分析,研究团队描绘出一条清晰的发育轨迹:csCAF很可能是iCAF的早期或前体状态。
亚型进行鉴定与表征.png)
图1. 利用scRNA-seq对人类癌相关成纤维细胞(CAF)亚型进行鉴定与表征
为了理解csCAF如何在肿瘤组织中发挥作用,研究采用了高分辨率时空组学技术Stereo-seq对这张“细胞地图”带来了更深入的洞察。
研究发现,csCAF富集的肿瘤区域,呈现出显著更健康的免疫微环境:抑制免疫的TGF-β信号水平更低,具有促瘤作用的M2型肿瘤相关巨噬细胞更少,而有益的脂质介质水平更高。
同时,研究还确定了csCAFs和T细胞之间存在空间定义的CXCL12-CXCR4配体-受体相互作用,且该相互作用模式在不同转移器官中存在差异。
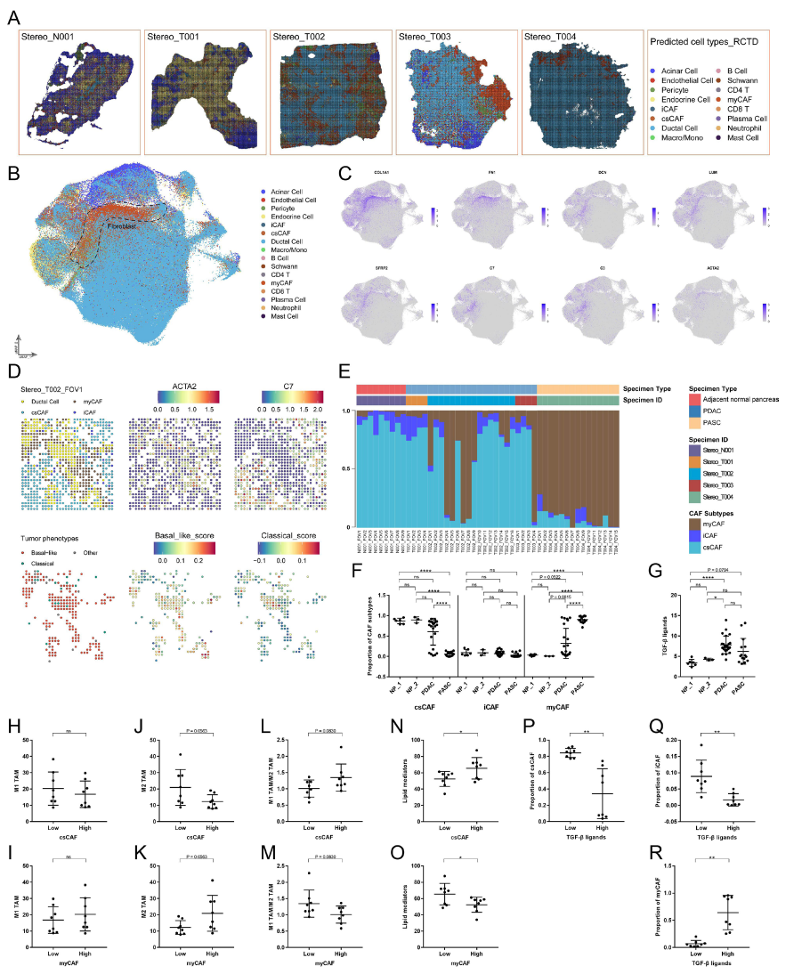
图2. Stereo-seq 揭示肿瘤内 CAF 的异质性
直接的临床价值:强大的预后保护伞
这项研究最令人振奋的发现,在于其明确的临床转化价值。通过对大规模临床样本的分析,研究一致证实:肿瘤组织中csCAF的比例越高,患者的总体生存期和无复发生存期显著越长。
这意味着,csCAF的比例可以作为一个强有力的预后生物标志物。此外,csCAF的比例与积极的临床特征紧密相关:在早期肿瘤、对新辅助化疗反应良好的患者中,csCAF的比例更高。
患者较好的临床预后相关.png)
图3. csCAFs 与胰腺导管腺癌(PDAC)患者较好的临床预后相关
基于以上发现,该研究提出了一个超越传统的颠覆性治疗策略:不再主张简单粗暴地清除所有CAF,而是精准地将“坏”的iCAF“重编程”回“好”的csCAF状态。这种“细胞功能正常化”的思路,代表了肿瘤治疗从“杀死癌细胞”到“改造肿瘤微环境”的深刻范式转变,与全球肿瘤研究的前沿方向高度契合。
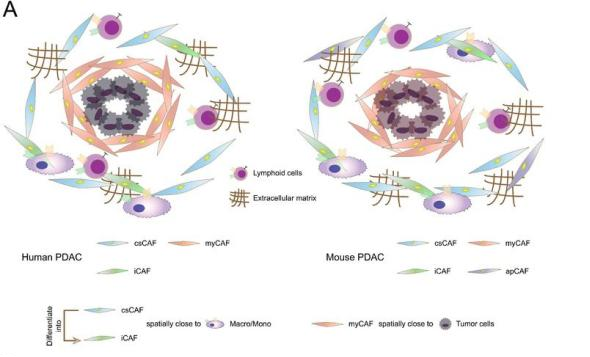
图4. 全面解析CAF的异质性谱与可塑性
这项研究不仅发现了一个与胰腺癌良好预后相关的关键细胞亚型(csCAF),阐明了其生物学特性及作为免疫微环境“保护伞”的机制,更重要的是,它指向了一条极具前景的临床转化路径——通过靶向CAF的可塑性,实现肿瘤微环境的“去恶化”和免疫功能的“再激活”。这为攻克胰腺癌这一顽疾,点燃了新的希望之光。
这项研究也是如何运用前沿生物技术解决复杂生物学问题的典范。它成功整合了单细胞转录组、单核多组学、时空组学(Stereo-seq)、多重免疫组化以及临床队列分析,形成了从分子机制、细胞互作、空间定位到临床验证的完整逻辑闭环。这种多维度、多尺度的研究框架,为未来肿瘤微环境研究提供了可借鉴的模板。


亚型进行鉴定与表征.png)

患者较好的临床预后相关.png)
