人类认知与记忆不仅依赖160亿个兴奋性神经元,更离不开作为“刹车系统”的抑制性神经元——它们负责平衡信号、防止过度兴奋,是构建高级神经环路的基石。进化中,人类抑制性神经元的数量比例和类型多样性远超其他物种,但其如何生成一直是神经科学未解的核心问题。
2026年1月15日,清华大学米达团队与中国医学科学院北京协和医院朱兰院士团队合作,在Science发表研究成果。该研究依托珍贵的人类胎儿样本,整合单细胞转录组、时空组学技术Stereo-seq等,系统绘制出人类大脑内侧神经节隆起(medial ganglionic eminence ,MGE)的细胞发育图谱。
该研究首次鉴定出灵长类特有的神经干细胞——脑室下区放射状胶质细胞(subventricular zone radial glial cell, SVZ RGC),阐明其可持续产生抑制性神经元与神经胶质细胞的核心功能,为解析人类大脑皮层的进化机制、开展神经发育疾病的干预研究提供了关键证据。
研究对象:多种物种脑组织样本(人类胎儿、食蟹猴、小鼠);
核心技术:单细胞 RNA 测序(scRNA-seq)、单细胞核 RNA 测序(snRNA-seq)、时空组学技术(Stereo-seq)、数字空间转录组(DSP)及免疫荧光染色与跨物种数据整合分析;
样本规模:单细胞转录组(覆盖GW9–GW39)、空间转录组(GW13、GW18、GW26)和数字空间转录组(GW18的21个特定区域)。实验验证覆盖数十例样本。研究还整合了小鼠和食蟹猴的胚胎脑数据进行跨物种比较。
灵长类特有!新型神经干细胞 SVZ RGC 被发现
研究整合时空组学技术Stereo-seq与单细胞转录组技术,系统描绘了人类胎儿MGE从GW9至GW39的发育景观,首次在人类MGE中发现新型神经干细胞——脑室下区放射状胶质细胞(SVZ RGC)。该细胞在分子特征、空间定位及分裂行为上均异于已知干细胞类型。
跨物种分析显示,SVZ RGC为灵长类特有。研究在食蟹猴MGE中鉴定出同源细胞群,但在小鼠中未见对应细胞类型。功能验证表明,SVZ RGC可持续产生GABA能抑制性神经元与胶质细胞,是人类大脑抑制性神经元数量及比例增加的关键细胞基础。
.png)
图1. 人类内侧神经节隆起脑室下区中的一种进化上独特的祖细胞类型(SVZ RGC)
人类大脑抑制性神经元多样性的时空发育机制
研究应用华大自主研发的时空组学技术Stereo-seq,首次在单细胞精度上绘制了人类MGE神经发生过程的时空转录图谱,揭示抑制性神经元多样性的核心机制。团队在人类MGE中划分出精细的神经祖细胞域,并明确其与五类抑制性神经元谱系的对应关系。
研究发现,神经元命运由其“出生地”和“出生时间”严格决定:发育早期,脑室区(VZ)的LHX8/ISL1、NR2F1/NR2F2祖细胞域主导神经发生;后期则转移至脑室下区(SVZ)的EPHA5/MEF2C、CRABP1/ANGPT2、LHX6/NFIA祖细胞域。这种“空间即命运”机制确保不同类型抑制性神经元在正确时间、按正确比例产生。
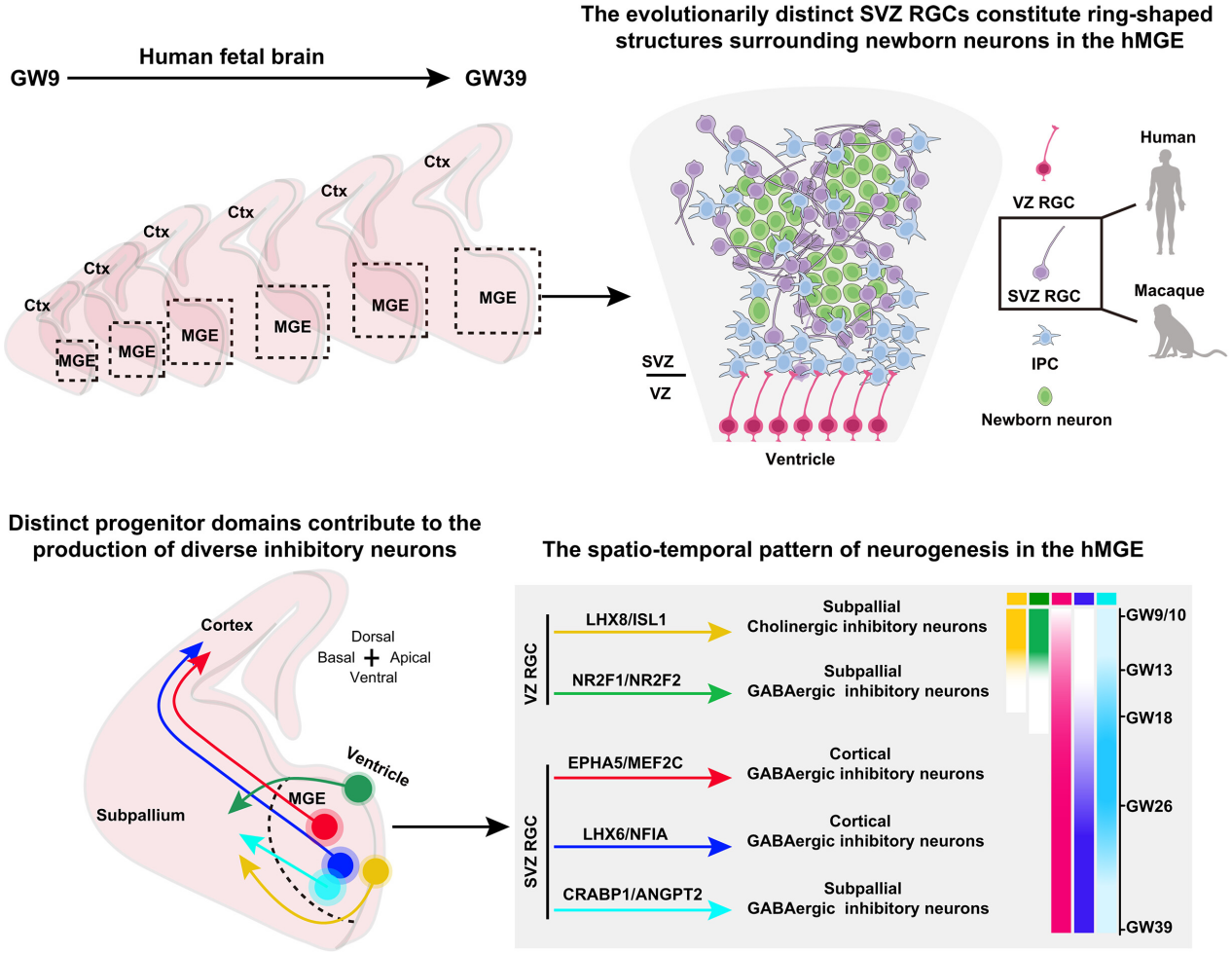
图2. 人类内侧神经节隆起神经发生的时空模式
研究提出“双引擎模型”,揭示人类大脑皮层扩张的逻辑:两种进化上独特的神经干细胞类型协同发挥作用。
两类干细胞协同工作,确保大脑兴奋-抑制网络平衡及高级认知功能的形成。
这项研究首次系统揭示了人类大脑抑制性神经元生成的进化独特机制,发现了SVZ RGC这一关键祖细胞类型,并阐明其在维持抑制性神经元长期生产中的核心作用。研究还建立了从祖细胞域到神经元谱系的时空图谱,并提出解释皮层进化的“双引擎模型”。这些发现不仅深化了人类对自身认知能力进化基础的理解,也为神经发育障碍(如自闭症、精神分裂症)的机制研究提供了新的细胞靶点和时空坐标系。
华大时空组学技术Stereo-seq凭借高分辨率空间转录组优势,实现了高通量转录组信息与组织原位的精准映射。一方面,其明确揭示新发现的SVZ RGCs 在空间上特异性定位于人类大脑内侧神经节隆起(MGE)的脑室下区(SVZ),与位于脑室区(VZ)的传统 RGCs 形成解剖学上的清晰区分,为两类 RGCs 的独立性提供了直接空间证据。
另一方面,通过整合 scRNA-seq 数据,成功将单细胞水平鉴定的细胞类型与其在发育大脑中的实际空间分布对应起来,填补了单细胞测序缺乏空间信息的空白,为“SVZ RGCs 是定位于 SVZ 的独特祖细胞”这一核心论点提供了关键的空间维度验证。


.png)
