胸腺作为T淋巴细胞发育与中枢免疫耐受建立的关键器官,其功能依赖于高度有序的空间微环境。传统单细胞测序技术虽能解析细胞类型,却丢失了空间位置信息;早期空间转录组技术分辨率有限,难以精确定位稀有细胞亚群。这导致胸腺内负责抗原模拟的稀有上皮细胞,其空间分布与功能机制长期未能阐明。
2026年3月,新加坡科学技术研究局下属的分子与细胞生物学研究所(A STAR IMCB)及新加坡国立大学(NUS)的研究团队,在Nature Communications发表研究成果。
研究依托华大智造DNBSEQ-Tx测序平台,采用时空组学技术Stereo-seq,结合单细胞测序与空间蛋白组学Stereo-CITE-seq等多模态分析,首次构建了从胎儿期(孕13-18周)至儿童期(7周-6岁)的人类胸腺高分辨率时空图谱。
时空组学技术Stereo-seq在本研究中实现了高分辨率(空间点直径25 µm,部分分析提升至10 µm)与大视场捕获(2 cm×3 cm芯片),完整解析了胸腺组织结构,为理解中枢免疫耐受的建立机制提供了全新的空间维度依据。

研究对象:人类胎儿期(孕13周、14周、17周、18周)和儿童期(7周龄、2岁、5岁、6岁)的胸腺组织;
核心技术:单细胞RNA测序和时空组学(Stereo-seq/Stereo-CITE-seq);
样本设计:对8个不同发育时间点的胸腺组织进行Stereo-seq空间转录组测序,并整合公共scRNA-seq数据。
关键研究发现
高清“地图”:胸腺细胞类型与区域精准定位
研究团队通过整合Stereo-seq空间转录组数据与单细胞RNA测序数据,对胸腺进行了系统性空间解析,确认了胸腺经典的皮质-髓质-间隔区三分结构,并依据基因表达特征,将其分为三个同心圆状功能亚区。
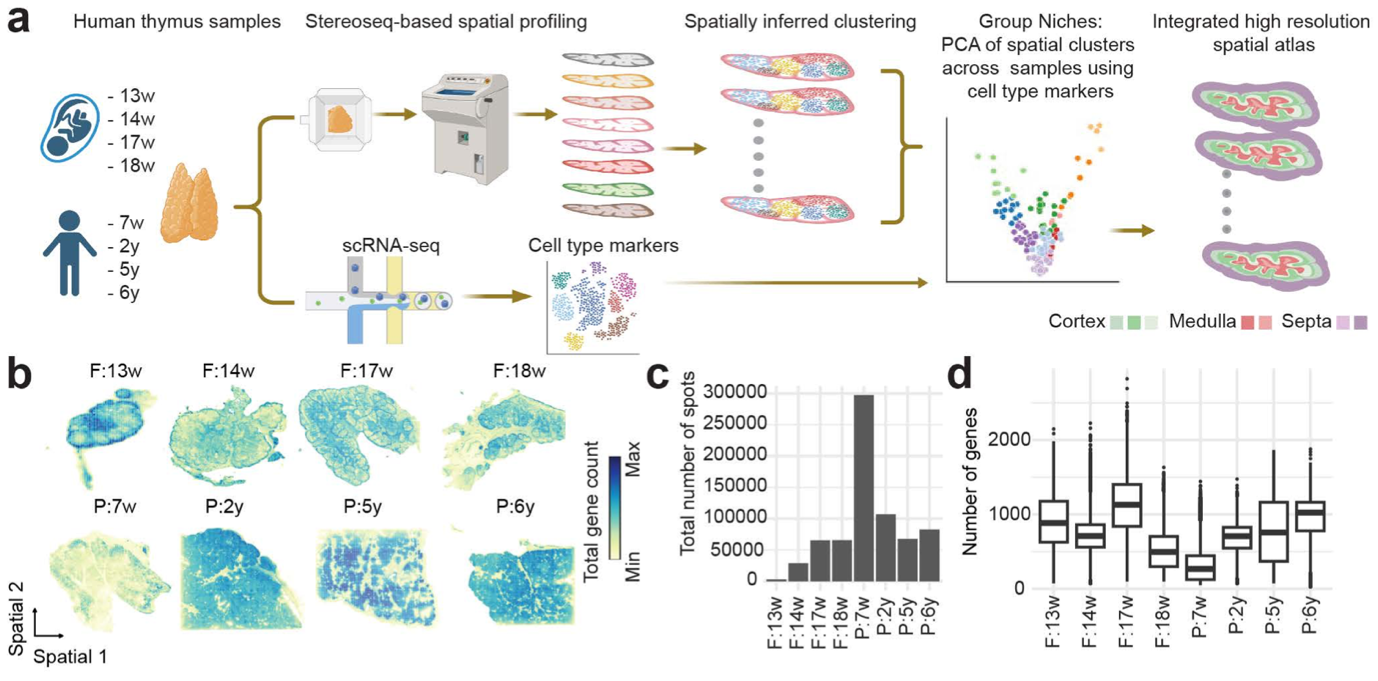
图1. 人类胎儿和儿童胸腺的高分辨率空间转录组图谱
空间映射结果显示,不同发育阶段的T细胞前体呈现从皮质外层向髓质内层有序迁移的分布模式:皮质区主要富集皮质胸腺上皮细胞(cTECs)和双阳性T(DPs)细胞;髓质区富集髓质胸腺上皮细胞(mTECs)、树突状细胞(DCs)及单阳性T细胞(SPs);成纤维细胞与内皮细胞则主要定位于间隔区,清晰揭示了胸腺各区域的细胞组成特征。
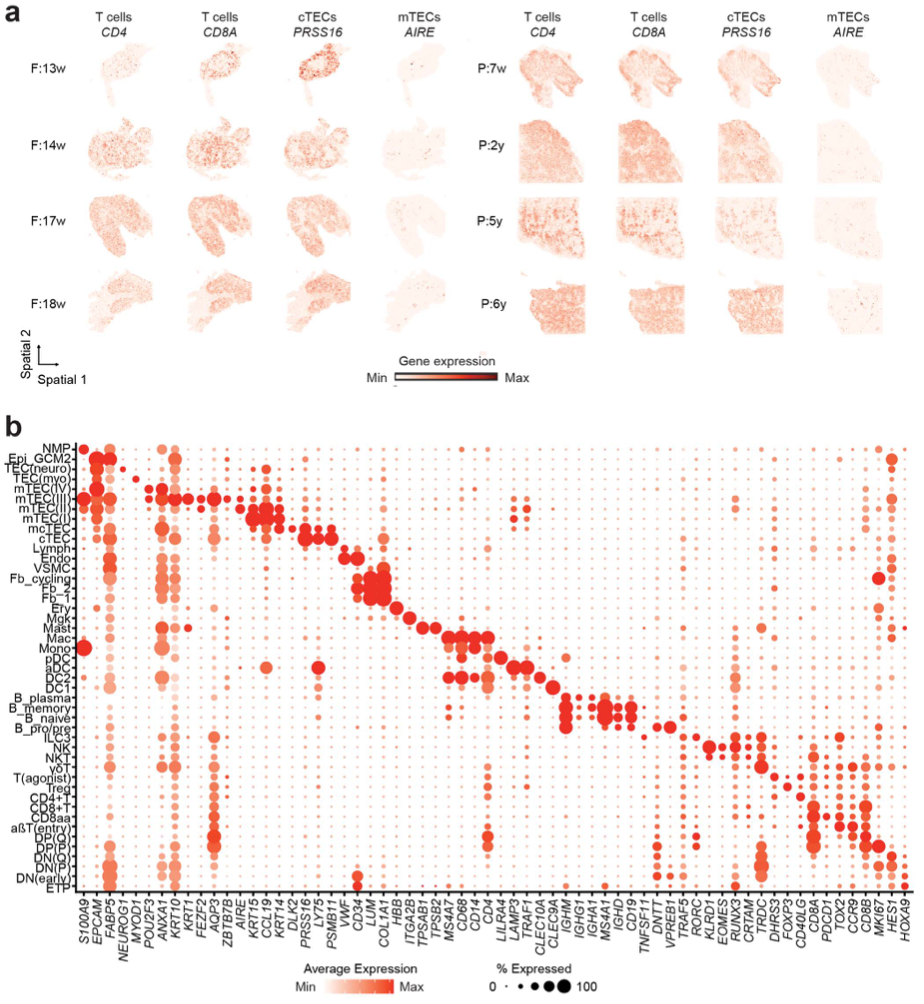
图2. 空间和单细胞转录组图谱中的标记基因表达谱
信号“对话”:驱动T细胞选择的关键通路
通过分析配体-受体对的共定位情况,研究揭示了胸腺微环境内特异的细胞间通讯网络,且该网络具有明显的区域特异性。在皮质区,成纤维细胞表达的CXCL12与T细胞前体表达的CXCR4形成的信号轴高度活跃,该信号通路被证实是引导T细胞前体向皮质归巢与驻留的关键;在髓质区,与淋巴细胞归巢(如CCL19-CCR7通路)、抗原提呈及T细胞激活(如MIF-CD74通路)相关的信号通路显著富集,与髓质作为T细胞阴性选择和成熟终末场所的功能定位高度契合。
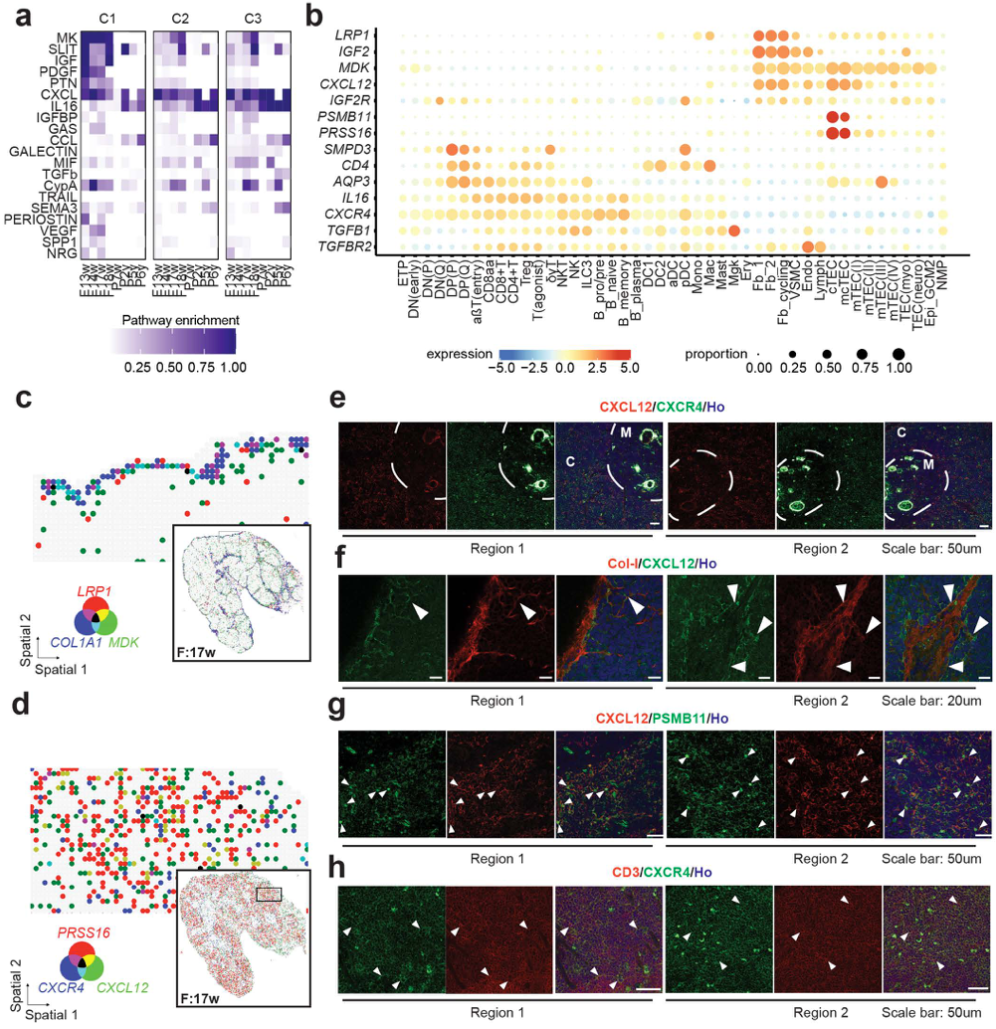
图3. 在T细胞阳性选择过程中活跃的信号通路
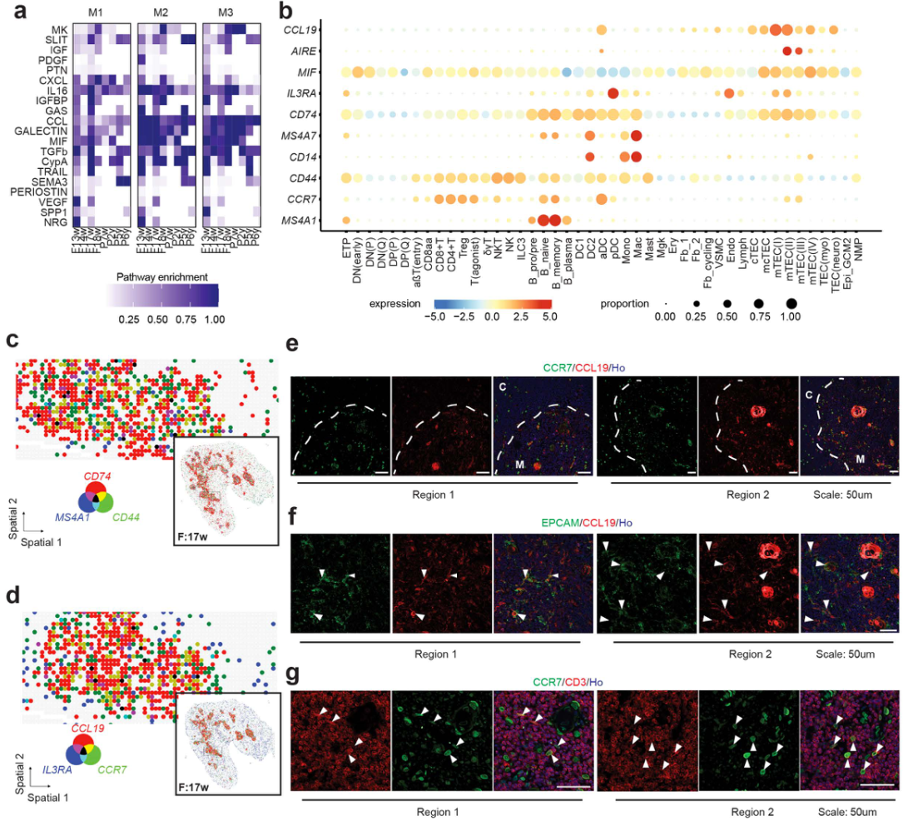
图4. 在T细胞阴性选择过程中活跃的信号通路
定位并解析罕见的“模仿胸腺上皮细胞”
这是本研究最具突破性的发现。借助Stereo-seq的高分辨率优势,研究人员成功从复杂胸腺组织中识别并定位了一类稀有且功能关键的模仿胸腺上皮细胞(TECs),定量分析显示其仅占所有检测空间位点的约0.4%。
空间分布上,这类细胞并非随机分布,而是高度聚集于胸腺髓质区的特定区域,尤其在哈索尔小体周围形成功能特化微域;分子特征上,研究鉴定出70余个该细胞特异性高表达的转录因子,不仅包含AIRE、FEZF2等已知的mTEC关键调控因子,还涵盖ASCL1(神经发育相关)、MYOG(肌肉发育相关)、INSM1(胰腺内分泌发育相关)等外周组织特异性转录因子。
这一发现从空间转录组层面提供直接证据,证实这类稀有mTEC可通过启动外周组织特征性基因表达程序,在胸腺内呈现广泛的自身抗原谱,为“胸腺通过模拟外周组织抗原以教育T细胞建立自身耐受”的理论假说,提供了坚实的分子与空间坐标依据。
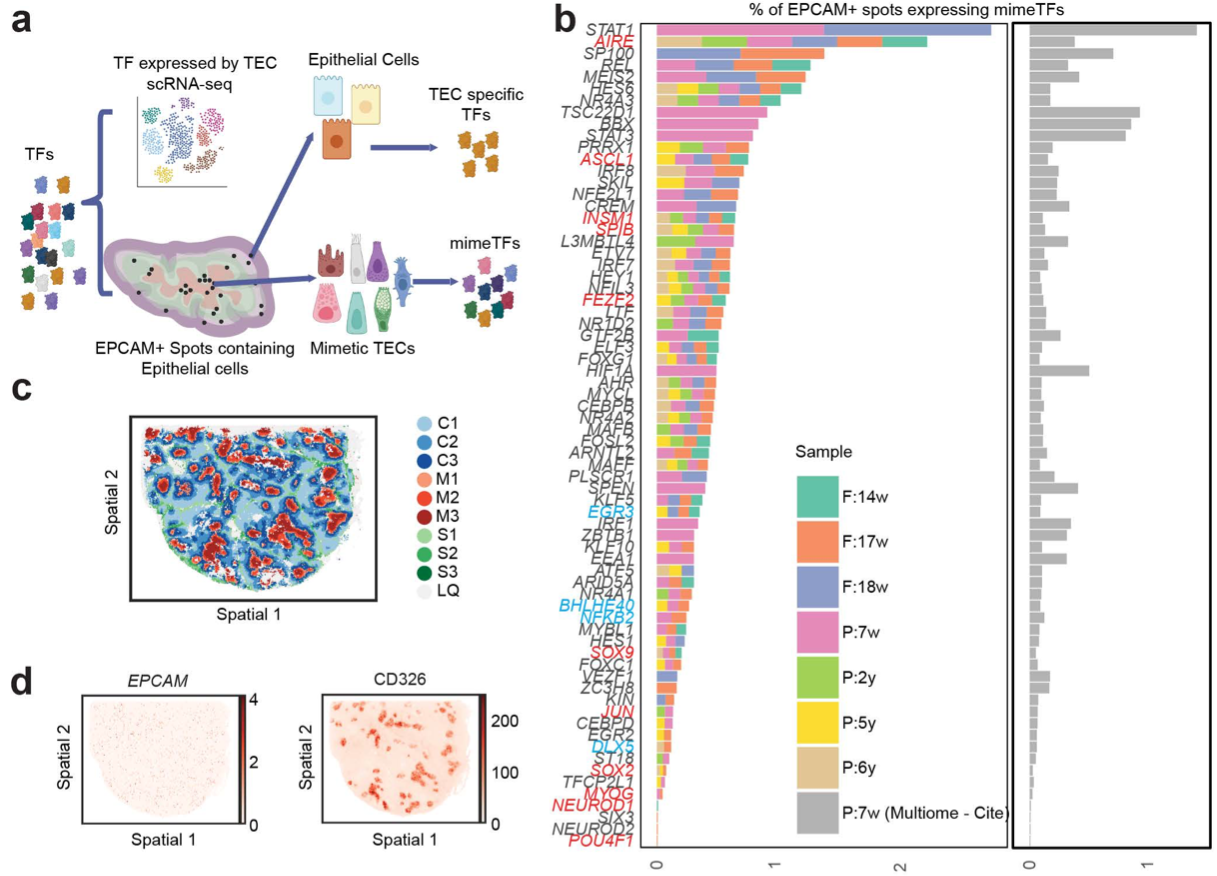
图5. 与稀有模仿胸腺上皮细胞(TECs)相关的转录因子的鉴定
本研究以华大时空组学技术Stereo-seq为核心,整合多模态分析方法,成功绘制了首张覆盖孕13周至6岁人类胸腺发育全周期的高精度时空图谱,突破了传统研究丢失空间信息的局限,将细胞类型、基因表达、信号通路与精确空间坐标有机结合,实现了对胸腺功能微环境的系统性、可视化解析。
该图谱作为重要的基础科研资源,为后续相关研究提供了基准框架:一方面,可作为参照,解析自身免疫性疾病、免疫缺陷、胸腺瘤等病理状态下,胸腺空间组织结构与细胞互作网络的紊乱机制;另一方面,为组织工程、细胞疗法等重建胸腺功能的研究,提供了关键细胞空间排布与分子对话的详细信息,具有重要的理论指导与实际应用价值。






