北京时间 4 月 17 日,国际顶尖学术期刊《科学》(Science)在线发表了由基因组多维解析技术全国重点实验室、杭州华大生命科学研究院、中国科学院脑科学与智能技术卓越创新中心、澳大利亚莫纳什大学等中外团队联合完成的重大突破成果。
依托华大智造的时空组学技术Stereo-seq、单细胞测序技术DNBelab C系列scRNA-seq技术,结合神经影像学(MRI),并基于DNBSEQ™测序平台完成高通量测序,研究团队不仅构建了全球首个狨猴全脑单细胞多模态图谱,还首次发现了灵长类大脑皮层中的Pr-Al对立分子梯度轴。这一发现为认知大脑结构、理解灵长类大脑高级认知功能的发育与演化提供了全新理论框架,还终结了学界关于大脑皮层演化近百年的争议。
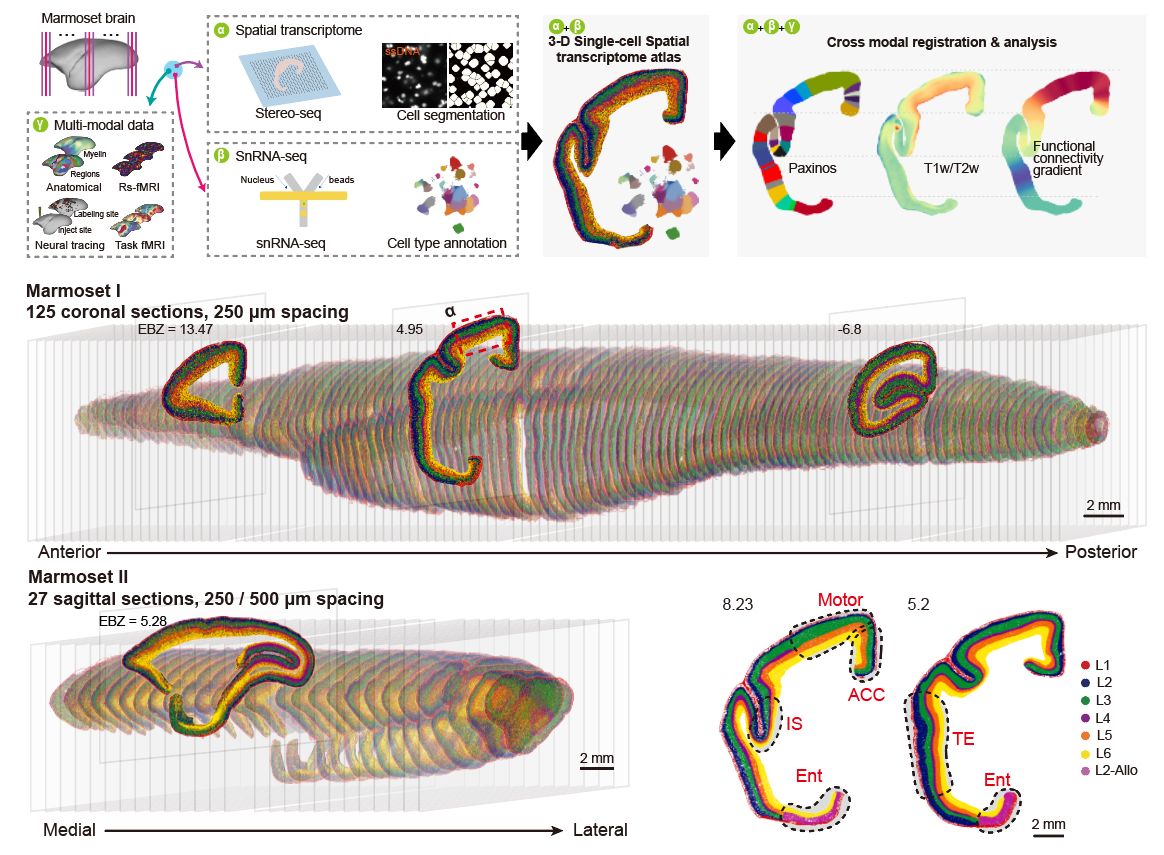
在以往的脑科学研究中,解剖学、影像学与基因组学往往相对独立,从各自维度切入,为解读大脑奥秘提供多元视角。而本研究通过将神经影像学(MRI)与华大智造时空组学技术Stereo-seq、单细胞测序技术 DNBelab C系列scRNA-seq技术深度融合,实现了宏观的功能监测与微观的分子解析紧密联动。
通过MRI,研究人员可以观测大脑在执行特定动作(如抓取或思考)时的实时活动情况;而利用时空组学技术Stereo-seq,就能像导航软件放大实景一样,精准锁定这些活动背后对应的细胞类型及其内部的基因表达;单细胞测序技术DNBelab C系列scRNA-seq 则助力研究团队完成超大规模单细胞核测序,精准解析49万余个细胞的转录组信息。
通过这种跨尺度、跨学科的整合,研究团队成功构建了全球首个狨猴全脑单细胞空间转录组+神经连接 + 功能影像的三维整合脑图谱,实现了分子表达、细胞类型、神经环路、解剖分区与功能网络的多维度精准对齐,让研究团队得以在全脑尺度系统解析皮层构建的底层逻辑。
目前,相关数据已保存至CNGBdb(MCCSTA 数据库)。
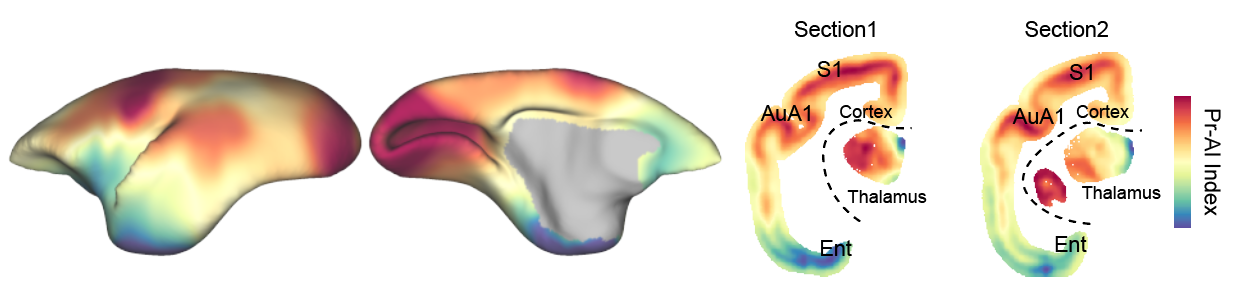
基于这张超高精度脑图谱,研究团队发现大脑皮层遵循一套精密的双向分子梯度轴:以Pr极(初级感觉区)与Al极(古皮层 / 边缘皮层)为对立演化锚点,两端各有大量基因高表达,并随空间延伸形成相向拮抗的分子梯度。
两股梯度交汇融合的中间区域,正是灵长类联合皮层——人类抽象思维、自我意识与高级决策的核心中枢。Pr-Al轴首次从分子层面解答了灵长类高级联合皮层的起源问题,统一了 “双起源假说” 与 “分子锚定假说”。该梯度轴不仅存在于大脑皮层,还贯穿丘脑、纹状体等全脑核团,构成全脑协同的演化逻辑。
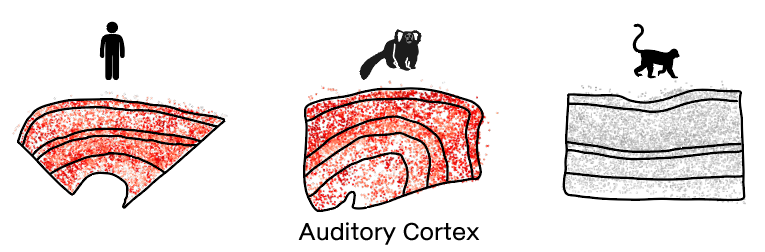
研究还发现一个与社交相关的重要结论:尽管猕猴在进化上与人类更近,但狨猴的听觉皮层分子特征却与人类更相似。这是因为狨猴具有复杂的社交发声行为,演化出了与人类高度共通的听觉-发声调控基因和细胞排布模式。依托时空组学技术与单细胞测序技术的精准解析,这一发现让狨猴成为研究人类语言起源、言语发育障碍及自闭症等社交相关疾病的理想动物模型。
本研究不仅终结了双起源假说与分子锚定假说的百年争议,更建立起一套从分子、细胞到核团、网络和演化的全层级、跨尺度脑构建理论。这一框架有望为自闭症、精神分裂症、阿尔茨海默病等脑疾病的诊断与干预提供全新靶点,也为类脑计算架构与人工智能系统勾勒了一份天然的设计蓝图。
在美国和日本的国家级脑计划中,狨猴都占据核心地位,是解析人类大脑、攻克脑疾病的理想实验模型。中国团队首次绘制狨猴脑图谱,成为“中国脑计划”的关键里程碑成果。单细胞和时空组学等技术,为这一成果的取得,提供了重要支撑。
单细胞测序技术能够以前所未有的分辨率解析大脑中数百种细胞类型的分子特征,揭示其转录组多样性;而时空组学技术则进一步将细胞类型精确定位于组织原位,绘制出细胞类型、基因表达和调控元件在三维脑区中的空间分布图谱。
两者的结合,实现了从分子、细胞到区域、网络的多尺度解析,不仅能系统揭示大脑皮层、屏状核、小脑等结构的细胞类型组成与空间组织规律,还能在发育、衰老、疾病(如脑出血、阿尔茨海默病)等动态过程中捕捉细胞状态与相互作用的时空演变。
值得一提的是,这并非时空组学技术与单细胞测序技术首次在顶级脑科学研究中发挥关键作用。2023年,研究人员基于该技术绘制了全球首个非人灵长类全脑皮层空间单细胞图谱,成果入选2023年度“中国神经科学重大进展”;2024年,该技术助力研究人员绘制了首个跨物种小脑空间转录组图谱,相关成果在Science发表;2025年,该技术进一步推动介观脑图谱大科学协作成果取得新突破。
点击查看介观脑图谱大科学计划专题成果
未来,华大智造的时空组学技术与单细胞测序技术,将持续支持科研人员从皮层结构解析到认知起源探索,层层解码人类脑这一生命最复杂的器官,推动中国在脑演化、脑认知与脑疾病研究领域不断迈向国际前沿,为全球脑科学发展提供核心工具支撑。
杭州华大生命科学研究院联合培养博士研究生黄智、联合培养硕士研究生李生龙,脑智卓越中心联合培养博士研究生杨倩倩、朱晓嘉、研究助理王贺、联合培养硕士研究生林霁煊为该论文的共同第一作者。杭州华大生命科学研究院副研究员郝世杰,中国科学院脑智卓越中心(神经科学研究所)研究员刘赐融、孙怡迪,澳大利亚莫纳什大学生物医学发现研究所教授 Marcello G.P.Rosa 为该论文的共同通讯作者。本研究所有研究方案与动物实验均严格遵循相关伦理要求与规定。